徕卡超分辨率gsdim显微镜的发展历史
纳米技术GSDIM (其次是个别分子返回基态枯竭显微镜) 提供详细的图像的蛋白质和其他生物分子在细胞内的空间布局。帮助向更多的研究实验室和成像中心的用户提供的GSDIM 技术市场上第一个商业系统 (徕卡 SR GSD) 是现在。利用超分辨率 GSDIM显微镜,细胞隔间和地区,如纤毛或单一的蛋白质,与他们互动的伙伴可以成像分辨率低于衍射极限,即在两位数纳米的范围,使得科学家们能更多地了解细胞内复杂的相互作用。时间,在这方面的知识可能导致更好的理解细胞以前无法治愈的疾病的原因。
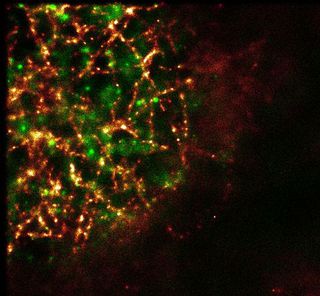
GSDIM 显微镜的原理
在传统的荧光显微镜中一种荧光染料的离域的 π 电子从地面状态 S0 转移到一种兴奋状态 S1。当他们回到基态 S0 振荡,他们发出的荧光光。GSDIM 技术,降低了通过切换到黑暗的状态 (图 1) (Fölling et al.,2008 年,Bierwagen et al.2010年,种皮 et al.,2010年) 大部分的荧光染料在此振荡周期中涉及的电子数目。这减少了可激发荧光团的数量,直到可以检测到单分子。单分子然后自发地从黑暗状态返回一个易激动的地面状态并发出荧光,而其他人都通过切换到黑暗状态再次停用。其结果是,荧光分子点亮或试样中"作祟"。单个荧光团的确切位置可以通过一种算法确定。所有的荧光团的位置信息收集在数千个单独的图像,其坐标用来计算超分辨率 GSDIM 图像。GSDIM 图像中所示的结构因此起源方式类似的流水账风格的绘画。
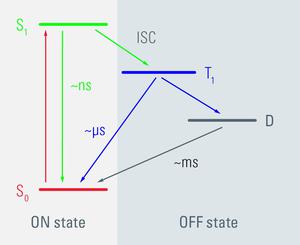
图 1: 基于一个简化的雅布伦斯基图的 GSDIM 方法的示意图。离域的 π 电子的荧光团可以是,例如,在地面状态 S0,在兴奋状态 S1 (既所谓的国家) 或三重态或激进黑暗状态 (这两个 OFF 状态)。当发出荧光光时,电子和流通,地面兴奋的状态。这些方面与国家不同,在关闭状态下的荧光团都不能够发出的光。这些 OFF 状态通常的使用寿命长,但他们是很难达到,由于国米系统过境所需。通过设置右环境条件嵌入介质中和通过的标准荧光免疫荧光为聪明的选择,有可能到可逆开关荧光团通过令人兴奋的他们与极端的光强度。当足够的分子在关闭状态下,有可能来检测样品中的个别分子。
首要的纤毛,非常规的细胞器为上皮细胞极性的组织
初级纤毛是在根尖表面的极化的上皮细胞,人体的细胞基于 microtubuli 的结构。这种形式的 monocilia 发现,例如,对种涂层的肾、 胆、 胰管上皮细胞。在这里他们发挥关键作用作为机械传感器 — — 例如,他们决定组成流体或他们的流动率(Fliegauf 等,2007年)。同时,他们也参与维持细胞极性,如有与梅丁达秘 (MDCK)犬肾细胞 (Bacallao 等,1989年) 图所示。初级纤毛形成在间期细胞周期从等离子膜相关依据约 250 毫微米宽叫做基底体,即轴丝形成这种结构 (Singla 等人,2006 年) 的基础上。基底身体的基本框架包括九个微管二聚体 (9 + 0)。各中心都设在这里,被视为基体的必要组成部分。这些蛋白质属于钙调素的家庭和有,他们是能够绑定Ca2 + EF 手主题 (索尔兹伯里,2007年)。Ca2 + 绑定所引起的构象变化调节与其他蛋白质如微管蛋白或半乳糖凝集素 3 中金的相互作用。有四种不同类型的金在小鼠和人的有机体。金-2 和-3 无所不在表示,并积累在中心粒和 pericentriolar 地区或在基底身体的单元格。金-1,另一方面,只发现胚芽细胞和视网膜,虽然金 4 只发现完全分化细胞 (索尔兹伯里,2007年)。
在 ciliogenesis 或纤毛的功能障碍是各种疾病,如视网膜变性、 多囊肾、 脑积水或BBS (Bardet-Biedl 综合征) 的原因。
蛋白质组分的基体在超分辨成像
徕卡SR GSD(徕卡显微系统,韦茨拉尔)是一个新的多用途的显微镜,不仅可用于超分辨率gsdim成像到20纳米的分辨率,同时也为TIRF显微镜(全内反射荧光)和高速宽视野的活细胞成像。这给了新的和非常详细的见解的根尖膜和蛋白质组成的结构。双染色Centrin-2与微管蛋白用免疫组织化学方法和成像技术的gsdim(图2A)。的微管网络下的顶膜可以清楚地可视化。其他可见的特点是半圆形的中央结构出现的每一次的细胞。设置在基体中,这些结构上还沾着Centrin-2。我们可以看到一个类似Centrin-2分布格局在此之前一样。图2b显示了一个双染结合伙伴Centrin-2 Galectin-3(科赫等人。,2010)。然而,传统的图像超分辨率图像提供了比gsdim更弥漫性的蛋白质分配观。
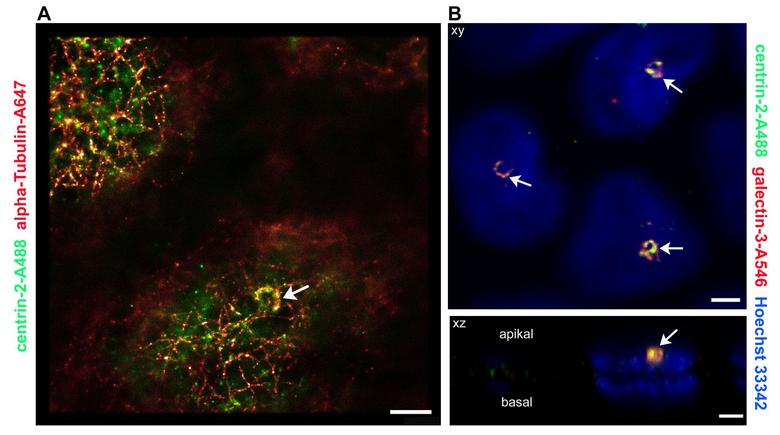
图2:超分辨率gsdim显微镜和激光共聚焦显微镜比较。A:gsdim显微镜(徕卡SR GSD),MDCK细胞培养在盖玻片,固定和染色anti-centrin-2 / A488和反α微管蛋白/ alexa647。在基体区微管蛋白和Centrin-2标签的半圆形结构(箭头)。规模:1µM。B:激光共聚焦显微镜(徕卡TCS SP2)扫描的顶端区域的MDCK细胞的免疫组化染色的anti-centrin-2 / A488和抗-galectin一3 / alexa546。核酸的细胞用Hoechst 33342染色。X / Y图像(上)再次显示了新月形的结构,也包含Centrin-2 Centrin-2的具有约束力的合作伙伴,Galectin-3(箭头)。X / Z图像清楚地显示这些结构位于顶部以上的细胞核。规模:1µM.
Outlook
GSDIM 技术产生了下面的衍射极限的细胞结构光显微成像技术的进一步突破。样品制备方法,相同的免疫组织化学方法可用于已建立在大多数实验室中衍射受限视场和共聚焦显微镜。政府物料供应处的显微镜可以显示已经看不见了到现在的结构。这可以被提供了更深的洞察力基本过程在细胞内的蛋白质和其合作伙伴的互动,高度详细成像技术。在将来,这种技术将用于获取新信息的细胞的原因以前无法医治的疾病。